2019年高考卷2理科綜合試題及參考答案整理!
高考卷2理科綜合適用于甘肅、青海、內蒙古、黑、吉林、遼寧、寧夏、新疆、陜西、重慶。這些地區的考生覺得考試難度怎么樣?物理化學生物三門科目的難度和考試強度都是對考生一個很大的考驗,慕羽茜2019年高考2卷的理科綜合試題還未公布,伊頓教育網小編為各位考生整理了2018年卷2的理科綜合試題內容和參考答案,后續將會更新2019年的試題內容。相關鏈接:2019年卷2理科綜合試題及參考答案!
2018年高考新課標Ⅱ(理綜)試卷
一、選擇題
1,下列關于人體中蛋白質功能的敘述,錯誤的是( ) A. 漿細胞產生的抗體可結合相應的病毒抗原
B. 肌細胞中的某些蛋白質參與肌肉收縮的過程
C. 蛋白質結合Mg2+形成的血紅蛋白參與O2運輸
D. 細胞核中某些蛋白質是染色體的重要組成成分
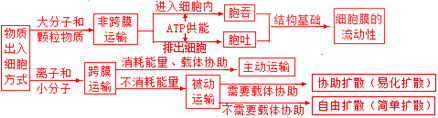
2,下列有關物質跨膜運輸的敘述,正確的是( ) A. 巨噬細胞攝入病原體的過程屬于協助擴散
B. 固醇類激素進入靶細胞的過程屬于主動運輸
C. 神經細胞受到刺激時產生的Na+內流屬于被動運輸
D. 護膚品中的甘油進入皮膚細胞的過程屬于主動運輸
3,下列有關人體內激素的敘述,正確的是( ) A. 運動時,腎上腺素水平升高,可使心率加快,說明激素是高能化合物
B. 饑餓時,胰高血糖素水平升高,促進糖原分解,說明激素具有酶的催化活性
C. 進食后,胰島素水平升高,其既可加速糖原合成,也可作為細胞的結構組分
D. 青春期,性激素水平升高,隨體液到達靶細胞,與受體結合可促進機體發育
4,有些作物的種子入庫前需要經過風干處理,與風干前相比,下列說法錯誤的是( ) A. 風干種子中有機物的消耗減慢
B. 風干種子上微生物不易生長繁殖
C. 風干種子中細胞呼吸作用的強度高
D. 風干種子中結合水與自由水的比值大
5,下列關于病毒的敘述,錯誤的是( ) A. 從煙草花葉病毒中可以提取到RNA
B. T2噬菌體可感染肺炎雙球菌導致其裂解
C. HIV可引起人的獲得性免疫缺陷綜合征
D. 阻斷病毒的傳播可降低其所致疾病的發病率
6,在致癌因子的作用下,正常動物細胞可轉變為癌細胞,有關癌細胞特點的敘述錯誤的是( ) A. 細胞中可能發生單一基因突變,細胞間黏著性增加
B. 細胞中可能發生多個基因突變,細胞的形態發生變化
C. 細胞中的染色體可能受到損傷,細胞的增殖失去控制
D. 細胞中遺傳物質可能受到損傷,細胞表面的糖蛋白減少
7,化學與生活密切相關。下列說法錯誤的是( ) A. 碳酸鈉可用于去除餐具的油污
B. 漂白粉可用于生活用水的消毒
C. 氫氧化鋁可用于中和過多胃酸
D. 碳酸鋇可用于胃腸X射線造影檢查
8, 研究表明,氮氧化物和二氧化硫在形成霧霾時與大氣中的氨有關(如下圖所示)。下列敘述錯誤的是( )
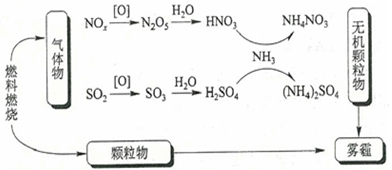
B. 霧霾中含有硝酸銨和硫酸銨
C. NH3是形成無機顆粒物的催化劑
D. 霧霾的形成與過度施用氮肥有關
9, 實驗室中用如圖所示的裝置進行甲烷與氯氣在光照下反應的實驗。
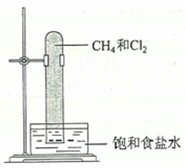
光照下反應一段時間后,下列裝置示意圖中能正確反映實驗現象的是( )
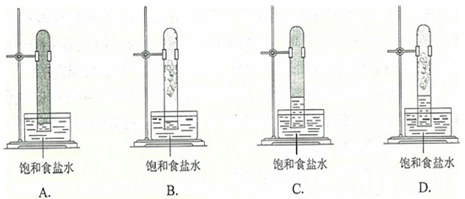
B. 如圖所示B
C. 如圖所示C
D. 如圖所示D
10,W、X、Y和Z為原子序數依次增大的四種短周期元素。W與X可生成一種紅棕色有刺激性氣味的氣體;Y的周期數是族序數的3倍;Z原子較外層的電子數與W的電子總數相同。下列敘述正確的是( ) A. X與其他三種元素均可形成兩種或兩種以上的二元化合物
B. Y與其他三種元素分別形成的化合物中只含有離子鍵
C. 四種元素的簡單離子具有相同的電子層結構
D. W的氧化物對應的水化物均為強酸
11,NA代表阿伏加德羅常數的值。下列說法正確的是( ) A. 常溫常壓下,124 g P4中所含P—P鍵數目為4NA
B. 100 mL 1mol•L−1FeCl3溶液中所含Fe3+的數目為0.1NA
C. 標準狀況下,11.2 L甲烷和乙烯混合物中含氫原子數目為2NA
D. 密閉容器中,2 mol SO2和1 mol O2催化反應后分子總數為2NA
12, 我國科學家研發了一種室溫下“可呼吸”的Na—CO2二次電池。將NaClO4溶于有機溶劑作為電解液,鈉和負載碳納米管的鎳網分別作為電極材料,電池的總反應為:3CO2+4Na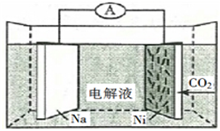
B. 充電時釋放CO2,放電時吸收CO2
C. 放電時,正極反應為:3CO2+4e− =D. 充電時,正極反應為:Na++e−=Na
13, 下列實驗過程可以達到實驗目的的是( )
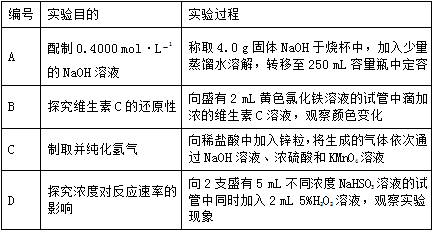
B. 如圖所示B
C. 如圖所示C
D. 如圖所示D
二、選擇題
14, 如圖,某同學用繩子拉動木箱,使它從靜止開始沿粗糙水平路面運動至具有某一速度,木箱獲得的動能( )
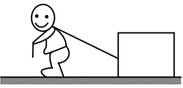
B. 等于拉力所做的功
C. 等于克服摩擦力所做的功
D. 大于克服摩擦力所做的功
15,高空墜物極易對行人造成傷害。若一個50g的雞蛋從一居民樓的25層墜下,與地面的撞擊時間約為2ms,則該雞蛋對地面產生的沖擊力約為( ) A. 10N
B. 102N
C. 103N
D. 104N
16,2018年2月,我國500m口徑射電望遠鏡(天眼)發現毫秒脈沖星“J0318+0253”,其自轉周期T=5.19ms,假設星體為質量均勻分布的球體,已知萬有引力常量為6.67×10−11N⋅m2/kg26.67×10−11N⋅m2/kg2。以周期T穩定自轉的星體的密度較小值約為( ) A. 5×109kg/m35×109kg/m3
B. 5×1012kg/m35×1012kg/m3
C. 5×1015kg/m35×1015kg/m3
D. 5×1018kg/m35×1018kg/m3
17,用波長為300nm的光照射鋅板,電子逸出鋅板表面的較大初動能為1.28××10-19J。已知普朗克常量為6.63××10-34J·s,真空中的光速為3.00××108m·s-1,能使鋅產生光電效應的單色光的較低頻率約為( ) A. 1××1014Hz
B. 8××1014Hz
C. 2××1015Hz
D. 8××1015Hz
18, 如圖,在同一平面內有兩根平行長導軌,導軌間存在依次相鄰的矩形勻強磁場區域,區域寬度均為l,磁感應強度大小相等、方向交替向上向下。一邊長為32l32l的正方形金屬線框在導軌上向左勻速運動,線框中感應電流i隨時間t變化的正確圖線可能是( )
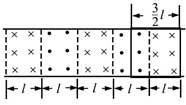
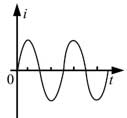
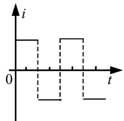
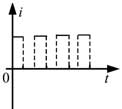
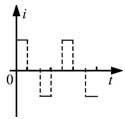
19, 甲、乙兩汽車同一條平直公路上同向運動,其速度—時間圖像分別如圖中甲、乙兩條曲線所示。已知兩車在t2時刻并排行駛,下列說法正確的是( )
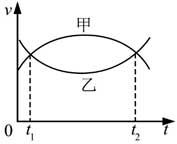
B. t1時刻甲車在后,乙車在前
C. 甲車的加速度大小先增大后減小
D. 乙車的加速度大小先減小后增大
20, 如圖,紙面內有兩條互相垂直的長直絕緣導線L1、L2,L1中的電流方向向左,L2中的電流方向向上;L1的正上方有a、b兩點,它們相對于L2對稱。整個系統處于勻強外磁場中,外磁場的磁感應強度大小為B0,方向垂直于紙面向外。已知a、b兩點的磁感應強度大小分別為13B013B0和12B012B0,方向也垂直于紙面向外。則( )
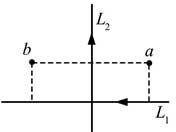
B. 流經L1的電流在a點產生的磁感應強度大小為112B0112B0
C. 流經L2的電流在b點產生的磁感應強度大小為112B0112B0
D. 流經L2的電流在a點產生的磁感應強度大小為712B0712B0
21, 如圖,同一平面內的a、b、c、d四點處于勻強電場中,電場方向與此平面平行,M為a、c連線的中點,N為b、d連線的中點。一電荷量為q(q>0)的粒子從a點移動到b點,其電勢能減小W1:若該粒子從c點移動到d點,其電勢能減小W2,下列說法正確的是( )
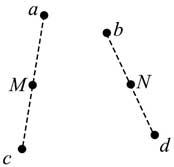
B. 若該粒子從M點移動到N點,則電場力做功為W1+W22W1+W22
C. 若c、d之間的距離為L,則該電場的場強大小為W2qLW2qL
D. 若W1=W2,則a、M兩點之間的電勢差等于b、N兩點之間的電勢差
三、非選擇題(一)考試題
22, 某同學組裝一個多用電表。可用的器材有:微安表頭(量程100 μ A, μ A,內阻900ΩΩ);電阻箱R1(阻值范圍0 ~ ~999.9ΩΩ);電阻箱R2(阻值范圍0 ~ ~99 999.9ΩΩ);導線若干。
要求利用所給器材先組裝一個量程為1mA的直流電流表,在此基礎上再將它改裝成量程為3V的直流電壓表。組裝好的多用電表有電流1mA和電壓3V兩擋。
回答下列問題:
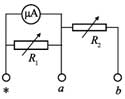
(1)在虛線框內畫出電路圖并標出R1和R2,其中*為公共接線柱,a和b分別是電流擋和電壓擋的接線柱______。
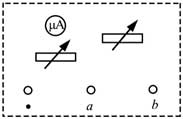
(2)電阻箱的阻值R1=R1=______ΩΩ;R2=______ΩΩ (保留到個位)23, 某同學用圖(a)所示的裝置測量木塊與木板之間的摩擦因數。跨過光滑定滑輪的細線兩端分別與木塊和彈簧秤相連,滑輪和木塊之間的細線保持水平,在木塊上放置砝碼。緩慢向左拉動水平放置的木板,當木塊和砝碼相對桌面靜止且木板仍在繼續滑動時,彈簧秤的示數即為木塊受到的滑動摩擦力的大小。某次實驗所得數據在下表中給出,其中f4f4的值從圖(b)中彈簧秤的示數讀出。
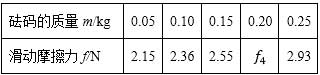
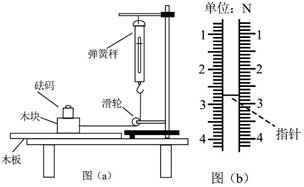
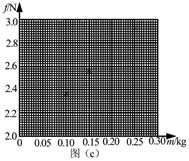
回答下列問題
(1)f4f4=______N
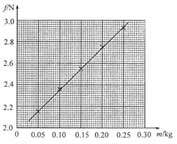
(2)在圖(c)的坐標紙上補齊未畫出的數據點______并繪出f-m圖線______;
(3)f與m、木塊質量M、木板和木塊之間的滑動摩擦因數μμ及重力加速度大小g之間的關系式f=______,f-m圖線(直線)的斜率的表達式k=____________;
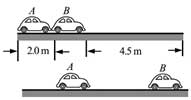
(4)取g=9.80 m/s2s2,由繪出的f-m圖線求得μ=______(保留2位有效數字)24, 汽車A在水平冰雪路面上行駛,駕駛員發現其正前方停有汽車B,立即采取制動措施,但仍然撞上了汽車B。兩車碰撞時和兩車都完全停止后的位置如圖所示,碰撞后B車向前滑動了4.5m,A車向前滑動了2.0m,已知A和B的質量分別為2.0×1032.0×103kg和1.5×1031.5×103kg,兩車與該冰雪路面間的動摩擦因數均為0.10,兩車碰撞時間極短,在碰撞后車輪均沒有滾動,重力加速度大小g=10m/s2g=10m/s2.求
(1)碰撞后的瞬間B車速度的大小;
(2)碰撞前的瞬間A車速度的大小。
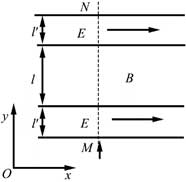
(1)定性畫出該粒子在電磁場中運動的軌跡;
(2)求該粒子從M點射入時速度的大小;
(3)若該粒子進入磁場時的速度方向恰好與x軸正方向的夾角為π6π6,求該粒子的比荷及其從M點運動到N點的時間。
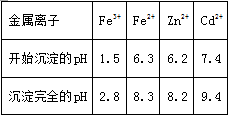
相關金屬離子[c0(Mn+)=0.1 mol•L-1]形成氫氧化物沉淀的pH范圍如下:
回答下列問題:
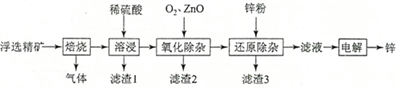
(1)焙燒過程中主要反應的化學方程式為______。
(2)濾渣1的主要成分除SiO2外還有______;氧化除雜工序中ZnO的作用是______,若不通入氧氣,其后果是______。
(3)溶液中的Cd2+可用鋅粉除去,還原除雜工序中反應的離子方程式為______。
(4)電解硫酸鋅溶液制備單質鋅時,陰極的電極反應式為______;沉積鋅后的電解液可返回______工序繼續使用。27, CH4-CO2催化重整不僅可以得到合成氣(CO和H2),還對溫室氣體的減排具有重要意義。回答下列問題:
(1)CH4-CO2催化重整反應為:CH4(g)+CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ•mol−1
C(s)+O2(g)=CO2(g) ΔH=-394 kJ•mol−1
C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ•mol−1
該催化重整反應的ΔH==______ kJ•mol−1。有利于增強CH4平衡轉化率的條件是______(填標號)。
A.高溫低壓
B.低溫高壓
C.高溫高壓
D.低溫低壓
某溫度下,在體積為2 L的容器中加入2 mol CH4、1 mol CO2以及催化劑進行重整反應,達到平衡時CO2的轉化率是50%,其平衡常數為______mol2•L−2。
(2)反應中催化劑活性會因積碳反應而降低,同時存在的消碳反應則使積碳量減少。
相關數據如下表:
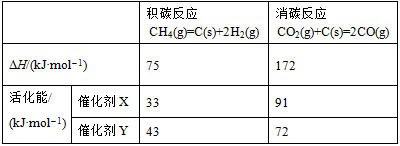
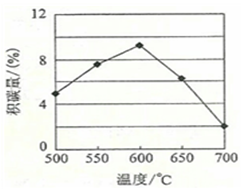
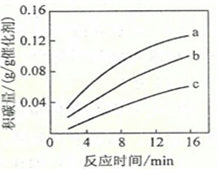
①由上表判斷,催化劑X______Y(填“優于”或“劣于”),理由是______。在反應進料氣組成、壓強及反應時間相同的情況下,某催化劑表面的積碳量隨溫度的變化關系如圖所示。升高溫度時,下列關于積碳反應、消碳反應的平衡常數(K)和速率(v)的敘述正確的是______填標號)。
A.K積、K消均增加
B.v積減小,v消增加
C.K積減小,K消增加
D.v消增加的倍數比v積增加的倍數大
②在溫度下,測得某催化劑上沉積碳的生成速率方程為v=k•p(CH4)•[p(CO2)]-0.5(k為速率常數)。在p(CH4)時,不同p(CO2)下積碳量隨時間的變化趨勢如圖所示,則pa(CO2)、pb(CO2)、pc(CO2)從大到小的順序為______。
(2)某小組為探究三草酸合鐵酸鉀的熱分解產物,按下圖所示裝置進行實驗。
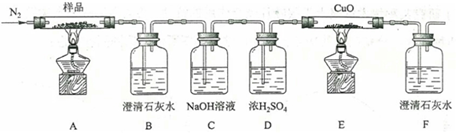
①通入氮氣的目的是______。
②實驗中觀察到裝置B、F中澄清石灰水均變渾濁,裝置E中固體變為紅色,由此判斷熱分解產物中含有______、______。
③為防止倒吸,停止實驗時應進行的操作是______。
④樣品完全分解后,裝置A中的殘留物含有FeO和Fe2O3,檢驗Fe2O3存在的方法是:______。
(3)測定三草酸合鐵酸鉀中鐵的含量。
①稱量m g樣品于錐形瓶中,溶解后加稀H2SO4酸化,用c mol•L-1 KMnO4溶液滴定至終點。滴定終點的現象是______。
②向上述溶液中加入過量鋅粉至反應完全后,過濾、洗滌,將濾液及洗滌液全部收集到錐形瓶中。加稀H2SO4酸化,用c mol•L-1 KMnO4溶液滴定至終點,消耗KMnO4溶液V mL。該晶體中鐵的質量分數的表達式為______。29, 為研究垂體對機體生長發育的作用,某同學用垂體切除法進行實驗。在實驗過程中,用幼齡大鼠為材料,以體重變化作為生長發育的檢測指標。回答下列問題:
(1)請完善下面的實驗步驟
①將若干只大鼠隨機分為A、B兩組后進行處理,A組(對照組)的處理是______,B組的處理是______。
②將上述兩組大鼠置于相同的適宜條件下飼養。
③______。
④對所得數據進行統計處理與分析
(2)實驗結果與分析
B組大鼠生長發育的狀況不如A組,出現這種差異的原因是由于B組的處理使大鼠缺失了來源于垂體的______激素和______激素。30, 為了研究某種樹木樹冠上下層葉片光合作用的特性,某同學選取來自樹冠不同層的A、B兩種葉片,分別測定其凈光合速率,結果如圖所示。據圖回答問題:
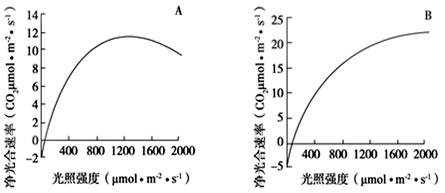
(1)從圖可知,A葉片是樹冠______(填“上層”或“下層”)的葉片,判斷依據是______。
(2)光照強度達到數值時,A葉片的凈光合速率開始下降,但測得放氧速率不變,則凈光合速率降低的主要原因是光合作用的______反應受到抑制。
(3)若要比較A、B兩種新鮮葉片中葉綠素的含量,在提取葉綠素的過程中,常用的有機溶劑是______。31, 大型肉食性動物對低營養級肉食性動物與植食性動物有捕食和驅趕作用。這一建立在“威懾”與“恐懼”基礎上的種間關系會對群落或生態系統產生影響,此方面的研究屬于“恐懼生態學”范疇。回答下列問題:
(1)當某種大型肉食性動物遷入到一個新的生態系統時,原有食物鏈的營養級有可能增加,生態系統中食物鏈的營養級數量一般不會太多,原因是______。
(2)如果將肉食性動物引入食物網只有三個營養級的某生態系統中,使得甲、乙兩種植食性動物間的競爭結果發生了反轉,即該生態系統中甲的數量優勢地位喪失。假定該反轉不是由于肉食性動物的直接捕食造成的,那么根據上述“恐懼生態學”知識推測,甲的數量優勢地位喪失的可能原因是______(答出一點即可)。
(3)若某種大型肉食性動物在某地區的森林中重新出現,會減輕該地區野豬對農作物的破壞程度。根據上述“恐俱生態學”知識推測,產生這一結果的可能原因有______(答出兩點即可)。32, 某種家禽的豁眼和正常眼是一對相對性狀,豁眼雌禽產蛋能力強。已知這種家禽的性別決定方式與雞相同,豁眼性狀由Z染色體上的隱性基因a控制,且在W染色體上沒有其等位基因。回答下列問題:
(1)用純合體正常眼雄禽與豁眼雌禽雜交,雜交親本的基因型為______。理論上F1個體的基因型和表現型為______, F2雌禽中豁眼禽所占的比例為______。
(2)為了給飼養場提供產蛋能力強的該種家禽,請確定一個合適的雜交組合,使其子代中雌禽均為豁眼,雄禽均為正常眼。寫出雜交組合和預期結果,要求標明親本和子代的表現型、基因型:______。
(3)假設M/m基因位于常染色體上,m基因純合時可使部分應表現為豁眼的個體表現為正常眼,而MM和Mm對個體眼的表現型無影響。以此推測,在考慮M/m基因的情況下,若兩只表現型均為正常眼的親本交配,其子代中出現豁眼雄禽,則親本雌禽的基因型為______,子代中豁眼雄禽可能的基因型包括______。(二)選考題
33,對于實際的氣體,下列說法正確的是______。 A. 氣體的內能包括氣體分子的重力勢能
B. 氣體的內能包括分子之間相互作用的勢能
C. 氣體的內能包括氣體整體運動的動能
D. 氣體體積變化時,其內能可能不變
E. 氣體的內能包括氣體分子熱運動的動能
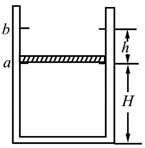
34, 如圖,一豎直放置的氣缸上端開口,氣缸壁內有卡口a和b,a、b間距為h,a距缸底的高度為H;活塞只能在a、b間移動,其下方密封有質量的理想氣體。已知活塞質量為m,面積為S,厚度可忽略;活塞和汽缸壁均絕熱,不計他們之間的摩擦。開始時活塞處于靜止狀態,上、下方氣體壓強均為p0,溫度均為T0。現用電熱絲緩慢加熱氣缸中的氣體,直至活塞剛好到達b處。求此時氣缸內氣體的溫度以及在此過程中氣體對外所做的功。重力加速度大小為g。
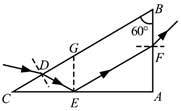
(i)求出射光相對于D點的入射光的偏角;
(ii)為實現上述光路,棱鏡折射率的取值應在什么范圍?37, 硫及其化合物有許多用途,相關物質的物理常數如下表所示:
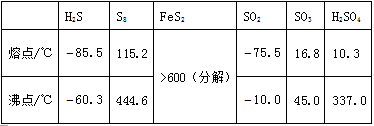
回答下列問題:
(1)基態Fe原子價層電子的電子排布圖(軌道表達式)為______,基態S原子電子占據較高能級的電子云輪廓圖為______形。
(2)根據價層電子對互斥理論,H2S、SO2、SO3的氣態分子中,中心原子價層電子對數不同于其他分子的是______。
(3)圖(a)為S8的結構,其熔點和沸點要比二氧化硫的熔點和沸點高很多,主要原因為______。
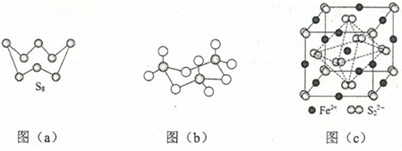
(4)氣態三氧化硫以單分子形式存在,其分子的立體構型為______形,其中共價鍵的類型有______種;固體三氧化硫中存在如圖(b)所示的三聚分子,該分子中S原子的雜化軌道類型為______。
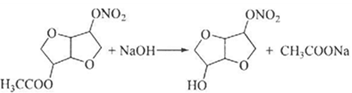
(5)FeS2晶體的晶胞如圖(c)所示。晶胞邊長為a nm、FeS2相對式量為M,阿伏加德羅常數的值為NA,其晶體密度的計算表達式為______g•cm−3;晶胞中Fe2+位于S2−2S22−所形成的正八面體的體心,該正八面體的邊長為______nm。38, 以葡萄糖為原料制得的山梨醇(A)和異山梨醇(B)都是重要的生物質轉化平臺化合物。E是一種治療心絞痛的藥物,由葡萄糖為原料合成E的過程如下:
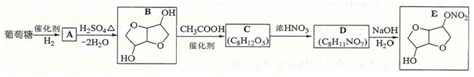
回答下列問題:
(1)葡萄糖的分子式為______。
(2)A中含有的官能團的名稱為______。
(3)由B到C的反應類型為______。
(4)C的結構簡式為______。
(5)由D到E的反應方程式為______。
(6)F是B的同分異構體,7.30 g的F與足量飽和碳酸氫鈉反應可釋放出2.24 L二氧化碳(標準狀況),F的可能結構共有______種(不考慮立體異構),其中核磁共振氫譜為三組峰,峰面積比為3∶1∶1的結構簡式為______。39, [生物——選修1:生物技術實踐]
在生產、生活和科研實踐中,經常通過消毒和滅菌來避免雜菌的污染。
回答下列問題:
(1)在實驗室中,玻璃和金屬材質的實驗器具______(填“可以”或“不可以”)放入干熱滅菌箱中進行干熱滅菌。
(2)牛奶的消毒常采用巴氏消毒法或高溫瞬時消毒法,與煮沸消毒法相比,這兩種方法的優點是______。
(3)密閉空間內的空氣可采用紫外線照射消毒,其原因是紫外線能______,在照射前,適量噴灑______,可強化消毒效果。
(4)水廠供應的自來水通常是經過______(填“氯氣”“乙醇”或“高錳酸鉀”)消毒的。
(5)某同學在使用高壓蒸汽滅菌鍋時,若壓力達到設定要求,而鍋內并沒有達到相應溫度,較可能的原因是______。40, [生物——選修3:現代生物科技專題]
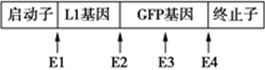
某種熒光蛋白(GFP)在紫外光或藍光激發下會發出綠色熒光,這一特性可用于檢測細胞中目的基因的表達。某科研團隊將某種病毒的外殼蛋白(L1)基因連接在GFP基因的5′末端,獲得了L1-GFP融合基因(簡稱為甲),并將其插入質粒P0,構建了真核表達載體P1,其部分結構和酶切位點的示意圖如下,圖中E1~E4四種限制酶產生的黏性末端各不相同。
回答下列問題:
(1)據圖推斷,該團隊在將甲插入質粒P0時,使用了兩種限制酶,這兩種酶是______。使用這兩種酶進行酶切是為了增加______,也是為了增加______。
(2)將P1轉入體外培養的牛皮膚細胞后,若在該細胞中觀察到了綠色熒光,則說明L1基因在牛的皮膚細胞中完成了______和______過程。
(3)為了獲得含有甲的牛,該團隊需要做的工作包括:將能夠產生綠色熒光細胞的______移入牛的______中、體外培養、胚胎移植等。
(4)為了檢測甲是否存在于克隆牛的不同組織細胞中,某同學用PCR方法進行鑒定。在鑒定時應分別以該牛不同組織細胞中的______(填“mRNA”“總RNA”或“核DNA”)作為PCR模板。
#p#副標題#e#
----參考答案----
【1題】
[答案]:C
[解析]: 由題意可知,該題考查的是蛋白質的功能的相關知識,選項所描述的是幾種常見的蛋白質的功能及其相關知識。
【詳解】
抗原能和特異性抗體相結合,病毒、細菌等病原體表面的蛋白質等物質,都可以作為引起免疫反應的抗原,可見,漿細胞產生的抗體可結合相應的病毒抗原,A正確;肌肉細胞中的某些蛋白質(如肌動蛋白等)參與肌肉收縮的過程,B正確;蛋白質結合Fe2+形成的血紅蛋白參與O2的運輸,C錯誤;染色體是細胞核的結構之一,染色體主要由DNA和蛋白質組成,D正確。
[點評]:【】
本題以蛋白質的功能為主線,綜合考查考生對體液免疫、組成肌肉細胞的肌動蛋白等蛋白質與血紅蛋白的功能、細胞核的結構及染色體的組成、無機鹽的功能等相關知識的識記和理解能力。解決此類問題,除了需要考生熟記并理解相關的基礎知識、形成知識網絡外,在平時的學習中要善于進行橫向聯系,即對教材中與某一知識有關的內容橫向輻射,進行歸納。
【2題】
[答案]:C
[解析]: 本題考查細胞的物質輸入與輸出,具體涉及了被動運輸(包括自由擴散和協助擴散)、主動運輸和胞吞等方式,意圖考查學生對相關知識點的理解能力。
【詳解】
病原體屬于顆粒性物質,顆粒性物質或大分子物質進出細胞的方式為胞吞和胞吐,因此巨噬細胞攝入病原體的過程屬于胞吞,A錯誤;固醇類激素的化學本質是脂質,脂溶性物質以自由擴散的方式進入靶細胞,B錯誤;神經細胞內的Na+濃度比細胞膜外低,受刺激時,產生的Na+內流是順濃度梯度進行的,屬于被動運輸,C正確;甘油是脂溶性小分子物質,以自由擴散的方式進入細胞,D錯誤。
[點評]:【】
【3題】
[答案]:D
[解析]: 由題意和選項的描述可知:該題考查激素調節及其實例(血糖調節)等相關知識。理清腎上腺素和性激素的功能、血糖調節過程、激素調節的特點是正確分析各選項的關鍵。
【詳解】
人體運動時,腎上腺素水平升高,給細胞傳達一種調節代謝的信息,引起心律加快,增加心輸出量,進而增強細胞代謝速率,為身體活動提供更多能量,可見激素不是高能化合物,而是信息分子,A錯誤;饑餓時,血糖濃度低,刺激胰島A細胞分泌更多的胰高血糖素,胰高血糖素與相應靶細胞膜上的受體結合,進而促進靶細胞內的糖原分解,但胰高血糖素不具有酶的催化活性,B錯誤;進食后,食物中的糖類經消化吸收導致血糖濃度升高,刺激胰島B細胞分泌更多的胰島素,胰島素通過促進葡萄糖進入組織細胞及其在組織細胞內氧化分解、合成糖原等生理過程而降低血糖濃度,但其不能作為細胞的結構組分,C錯誤;青春期,性腺分泌的性激素水平升高,性激素隨體液運輸到達靶細胞,與相應的受體結合,促進生殖器官的發育以及生殖細胞的形成,D正確。
[點評]:【】
激素是一種信號分子,既不組成細胞結構,又不提供能量,也不起催化作用,而是隨體液到達靶細胞,使靶細胞原有的生理活動發生變化。
【4題】
[答案]:C
[解析]: 由題文“種子入庫前需要經過風干處理”可知,該題考查的是水的存在形式及其與細胞呼吸等代謝活動的關系。
【詳解】
風干的種子中自由水含量極少,細胞呼吸作用強度弱,因此有機物消耗減慢,A正確,C錯誤;風干的種子含水量少,不利于微生物的生長繁殖,B正確;風干的種子中自由水含量極少,導致結合水與自由水的比值增大,D正確。
[點評]:【】
種子風干的過程中自由水含量逐漸降低。在范圍內,自由水與結合水比值的大小決定了細胞或生物體的代謝強度:比值越大說明細胞(或生物體)中自由水含量越多,代謝越強;反之,代謝越弱。
【5題】
[答案]:B
[解析]: 本題以“病毒”為情境,考查了幾種常見的DNA病毒和RNA病毒及其宿主等相關內容,選項命題角度新穎,試題較易。
【詳解】
煙草花葉病毒的遺傳物質是RNA,因此從煙草花葉病毒中可以提取到RNA,A正確;T2噬菌體是一種寄生在大腸桿菌體內的病毒,可見,T2噬菌體可感染大腸桿菌導致其裂解,B錯誤;艾滋病的全稱是獲得性免疫缺陷綜合征,其發病機理是HIV病毒主要侵染T細胞,使機體幾乎喪失一切免疫功能,C正確;阻斷病毒的傳播,是保護易感人群的有效措施之一,可降低其所致疾病的發病率,D正確。
[點評]:【】
根據遺傳物質的不同,將病毒分為DNA病毒(如T2噬菌體)和RNA病毒(如煙草花葉病毒、流感病毒、HIV等)。T2噬菌體是一種寄生在大腸桿菌體內的病毒,HIV病毒主要侵染T細胞,導致人患獲得性免疫缺陷綜合征。
【6題】
[答案]:A
[解析]: 依題意可知:本題是對細胞癌變的原因及其癌細胞特點的考查。理清相應的基礎知識、形成清晰的知識網絡,據此分析各選項。
【詳解】
細胞癌變的發生并不是單一基因突變的結果,而是一系列的原癌基因與抑癌基因的變異逐漸積累的結果,癌細胞的形態結構發生顯著變化,其細胞膜上的糖蛋白減少,細胞間的黏著性降低,A錯誤,B正確;原癌基因主要負責調節細胞周期,控制細胞生長和分裂的進程,抑癌基因主要是阻止細胞不正常的增殖,如果細胞中的染色體受到損傷,導致原癌基因或抑癌基因隨著它們所在的染色體片段一起丟失,則可能會出現細胞的增殖失去控制,C正確;綜上分析,癌細胞中遺傳物質(DNA)可能受到損傷,細胞表面的糖蛋白減少,D正確。
[點評]:【】
本題的易錯點在于:誤認為只要相關的單一基因突變就能引發細胞癌變;事實上,細胞癌變是一系列的原癌基因與抑癌基因的變異逐漸積累的結果。本題的難點在于對C 選項中的“染色體可能受到損傷”的理解;如果能聯想到“基因與染色體的位置存在平行關系”,則會有一種“豁然開朗”的感覺。
【7題】
[答案]:D
[解析]: A. 碳酸鈉水解溶液顯堿性,因此可用于去除餐具的油污,A正確;
B. 漂白粉具有強氧化性,可用于生活用水的消毒,B正確;
C. 氫氧化鋁是兩性氫氧化物,能與酸反應,可用于中和過多胃酸,C正確;
D. 碳酸鋇難溶于水,但可溶于酸,生成可溶性鋇鹽而使蛋白質變性,所以不能用于胃腸X射線造影檢查,應該用硫酸鋇,D錯誤。答案選D。
[點評]:【分析】
A.碳酸鈉溶液顯堿性;
B.漂白粉具有強氧化性;
C.氫氧化鋁能與酸反應;
D.碳酸鋇可溶于酸。
【教育】
本題主要是考查常見化學物質的性質和用途判斷,題目難度不大。平時注意相關基礎知識的積累并能靈活應用即可,注意碳酸鋇與硫酸鋇的性質差異。
【8題】
[答案]:C
[解析]: A. 霧的分散劑是空氣,分散質是水。霾的分散劑是空氣,分散質固體顆粒。因此霧和霾的分散劑相同,A正確;
B. 由于氮氧化物和二氧化硫轉化為銨鹽形成無機顆粒物,因此霧霾中含有硝酸銨和硫酸銨,B正確;
C. NH3作為反應物參加反應轉化為銨鹽,因此氨氣不是形成無機顆粒物的催化劑,C錯誤;
D. 氮氧化物和二氧化硫在形成霧霾時與大氣中的氨有關,由于氮肥會釋放出氨氣,因此霧霾的形成與過度施用氮肥有關,D正確。答案選C。
[點評]:【分析】
A.霧和霾的分散劑均是空氣;
B.根據示意圖分析;
C.在化學反應里能改變反應物化學反應速率(增強或降低)而不改變化學平衡,且本身的質量和化學性質在化學反應前后都沒有發生改變的物質叫催化劑;
D.氮肥會釋放出氨氣。
【教育】
結合示意圖的轉化關系明確霧霾的形成原理是解答的關鍵,氨氣作用判斷是解答的易錯點。本題情境真實,應用導向,聚焦學科素養,既可以引導考生認識與化學有關的社會熱點問題,形成可持續發展的意識和綠色化學觀念,又體現了高考評價體系中的應用性和綜合性考查要求。
【9題】
[答案]:D
[解析]: 在光照條件下氯氣與甲烷發生取代反應生成氯化氫和四種氯代烴,氯化氫極易溶于水,所以液面會上升。但氯代烴是不溶于水的氣體或油狀液體,所以較終水不會充滿試管,答案選D。
[點評]:【分析】
在光照條件下氯氣與甲烷發生取代反應生成氯化氫和四種氯代烴,結合有關物質的溶解性分析解答。
【教育】
明確甲烷發生取代反應的原理和有關物質的溶解性是解答的關鍵,本題取自教材中學生比較熟悉的實驗,難度不大,體現了依據大綱,回歸教材,考查學科收藏知識,體現高考評價體系中的基礎性考查要求。
【10題】
[答案]:A
[解析]: 根據以上分析可知W、X、Y和Z分別是N、O、Na、Cl。則
A. 氧元素與其N、Na、Cl三種元素均可形成兩種或兩種以上的二元化合物,例如NO、NO2、Na2O、Na2O2、Cl2O7、ClO2等,A正確;
B. 過氧化鈉中含有離子鍵和共價鍵,B錯誤;
C. N、O、Na三種元素的簡單離子具有相同的電子層結構,均是10電子,氯離子是18電子微粒,C錯誤;
D. 亞硝酸為弱酸,D錯誤。答案選A。
[點評]:【分析】
W、X、Y和Z為原子序數依次增大的四種短周期元素。W與X可生成一種紅棕色有刺激性氣味的氣體,W是N,X是O;Y的周期數是族序數的3倍,因此Y只能是第三周期,所以Y是Na;Z原子較外層的電子數與W的電子總數相同,Z的較外層電子數是7個,Z是Cl,結合元素周期律和物質的性質解答。
【教育】
本題考查元素周期表和元素周期律的知識,準確判斷出元素是解答的關鍵,紅棕色氣體是解答的沖刺點,該類試題與元素化合物的知識結合的比較多,元素推斷只是一種載體,注意掌握常見單質及其化合物的性質、典型用途、制備等。
【11題】
[答案]:C
[解析]: A. 常溫常壓下,124 g P4的物質的量是1mol,由于白磷是正四面體結構,含有6個P-P鍵,因此其中所含P—P鍵數目為6NA,A錯誤;
B. 鐵離子在溶液中水解,所以100 mL 1mol•L−1FeCl3溶液中所含Fe3+的數目小于0.1NA,B錯誤;
C. 甲烷和乙烯分子均含有4個氫原子,標準狀況下,11.2 L甲烷和乙烯混合物的物質的量是0.5mol,其中含氫原子數目為2NA,C正確;
D. 反應2SO2+O2[點評]:【分析】
A.根據白磷是正四面體結構分析;
B.根據鐵離子水解分析;
C.根據甲烷和乙烯均含有4個氫原子分析;
D.根據反應是可逆反應判斷。
【教育】
本題主要是考查阿伏加德羅常數的應用,是高考的一個高頻考點,主要從物質結構、水解、轉移電子、可逆反應等角度考查,本題相對比較容易,只要認真、細心就能做對,平時多注意這方面的積累。白磷的結構是解答的難點,注意與甲烷正四面體結構的區別。
【12題】
[答案]:D
[解析]: A. 放電時是原電池,陰離子[點評]:【分析】
原電池中負極發生失去電子的氧化反應,正極發生得到電子的還原反應,陽離子向正極移動,陰離子向負極移動,充電可以看作是放電的逆反應,據此解答。
【教育】
本題以我國科學家發表在化學刊物上的“一種室溫下可呼吸的鈉、二氧化碳二次電池”為載體考查了原電池和電解池的工作原理,掌握原電池和電解池的工作原理是解答的關鍵,注意充電與發電關系的理解。本題很好的弘揚了社會主義價值觀個人層面的愛國精神,落實了立德樹人的教育根本任務。
【13題】
[答案]:B
[解析]: A.氫氧化鈉溶于水放熱,因此溶解后需要冷卻到室溫下再轉移至容量瓶中,A錯誤;
B.氯化鐵具有氧化性,能被維生素C還原為氯化亞鐵,從而使溶液顏色發生變化,所以向盛有2 mL黃色氯化鐵溶液的試管中滴加濃的維生素C溶液,通過觀察顏色變化可以探究維生素C的還原性,B正確;
C.向稀鹽酸中加入鋅粒,生成氫氣,由于生成的氫氣中含有氯化氫和水蒸氣,因此將生成的氣體依次通過NaOH溶液、濃硫酸即可,不需要通過KMnO4溶液,或者直接通過堿石灰,C錯誤;
D.反應的方程式為[點評]:【分析】
A.氫氧化鈉溶于水放熱;
B.根據鐵離子具有氧化性結合溶液顏色變化分析;
C.氫氣中含有氯化氫和水蒸氣,據此解答;
D.根據雙氧水與亞硫酸氫鈉反應的實驗現象分析。
【教育】
明確相關物質的性質特點、發生的反應和實驗原理是解答的關鍵。注意設計或評價實驗時主要從正確與錯誤、嚴密與不嚴密、準確與不準確、可行與不可行等方面作出判斷。另外有無干擾、是否經濟、是否安全、有無污染等也是要考慮的。本題中選項D是解答的易錯點,學生往往只考慮物質的濃度不同,而忽略了實驗結論需要建立在實驗現象的基礎上。
【14題】
[答案]:A
[解析]: 受力分析,找到能影響動能變化的是那幾個物理量,然后觀測這幾個物理量的變化即可。
木箱受力如圖所示:
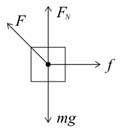
木箱在移動的過程中有兩個力做功,拉力做正功,摩擦力做負功,
根據動能定理可知即:WF−Wf=12mv2−0WF−Wf=12mv2−0 ,所以動能小于拉力做的功,故A正確;無法比較動能與摩擦力做功的大小,CD錯誤。故選A
[點評]:【】:
正確受力分析,知道木箱在運動過程中有那幾個力做功且分別做什么功,然后利用動能定理求解末動能的大小。
【15題】
[答案]:C
[解析]: 本題是一道估算題,所以大致要知道一層樓的高度約為3m,可以利用動能定理或者機械能守恒求落地時的速度,并利用動量定理求力的大小。
設雞蛋落地瞬間的速度為v,每層樓的高度大約是3m,
由動能定理可知:mgh=12mv2mgh=12mv2 ,
解得:v=2gh−−−√=2×10×3×25−−−−−−−−−−−−−√=1015−−√m/sv=2gh=2×10×3×25=1015m/s
落地時受到自身的重力和地面的支持力,規定向上為正,
由動量定理可知:(N−mg)t=0−(−mv)(N−mg)t=0−(−mv) ,解得:N≈1000NN≈1000N ,
根據牛頓第三定律可知雞蛋對地面產生的沖擊力約為103N,故C正確。故選C
[點評]:【】:
利用動能定理求出落地時的速度,然后借助于動量定理求出地面的接觸力
【16題】
[答案]:C
[解析]: 在天體中萬有引力提供向心力,即GMmR2=m(2πT)2RGMmR2=m(2πT)2R,天體的密度公式ρ=MV=M43πR3ρ=MV=M43πR3,結合這兩個公式求解。
設脈沖星質量為M,密度為ρρ
根據天體運動規律知:GMmR2≥m(2πT)2RGMmR2≥m(2πT)2R
ρ=MV=M43πR3ρ=MV=M43πR3
代入可得:ρ≈5×1015kg/m3ρ≈5×1015kg/m3 ,故C正確;故選C
[點評]:【】:
根據萬有引力提供向心力并結合密度公式ρ=MV=M43πR3ρ=MV=M43πR3求解即可。
【17題】
[答案]:B
[解析]: 知道光電效應方程Ek=hν−W0Ek=hν−W0;知道逸出功W0=hν0W0=hν0并結合兩個公式求解。
由光電效應方程式得:
Ek=hν−W0Ek=hν−W0
得:W0=hν−Ek=hcλ−EkW0=hν−Ek=hcλ−Ek
剛好發生光電效應的臨界頻率為ν0ν0
則W0=hν0W0=hν0
代入數據可得:ν0=8×1014Hzν0=8×1014Hz ,故B正確;故選B
[點評]:【】:
本題比較簡單,知道光電效應方程并利用方程求解即可。
【18題】
[答案]:D
[解析]: 找到線框在移動過程中誰切割磁感線,并根據右手定則判斷電流的方向,從而判斷整個回路中總電流的方向。要分過程處理本題。
第一過程從①移動②的過程中
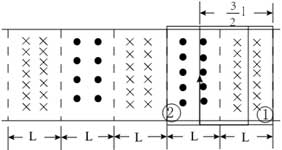
左邊導體棒切割產生的電流方向是順時針,右邊切割磁感線產生的電流方向也是順時針,兩根棒切割產生電動勢方向相同所以E=2BlvE=2Blv,則電流為i=ER=2BlvRi=ER=2BlvR,電流恒定且方向為順時針,
再從②移動到③的過程中左右兩根棒切割磁感線產生的電流大小相等,方向相反,所以回路中電流表現為零,
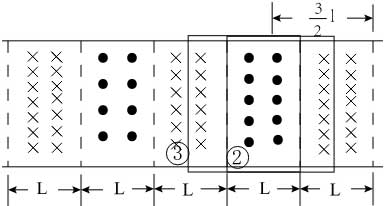
然后從③到④的過程中,左邊切割產生的電流方向逆時針,而右邊切割產生的電流方向也是逆時針,所以電流的大小為i=ER=2BlvRi=ER=2BlvR,方向是逆時針
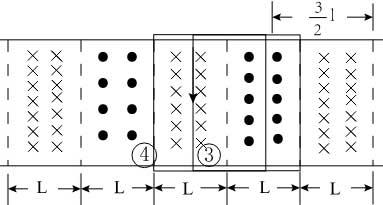
當線框再向左運動時,左邊切割產生的電流方向順時針,右邊切割產生的電流方向是逆時針,此時回路中電流表現為零,故線圈在運動過程中電流是周期性變化,故D正確;故選D
[點評]:【】:
根據線圈的運動利用楞次定律找到電流的方向,并計算電流的大小從而找到符合題意的圖像。
【19題】
[答案]:B,D
[解析]: 在v-t圖像中圖像包圍的面積代表了運動走過的位移,圖像的斜率代表加速度,解本題要利用這個知識點求解。
AB,v-t圖像中圖像包圍的面積代表運動走過的位移,兩車在t2時刻并排行駛,利用逆向思維并借助于面積可知在t1時刻甲車在后,乙車在前,故A錯誤,B正確;
CD、圖像的斜率表示加速度,所以甲的加速度先減小后增大,乙的加速度也是先減小后增大,故C錯D正確;故選BD
[點評]:【】:
本題考查了對圖像的理解及利用圖像解題的能力問題
【20題】
[答案]:A,C
[解析]: 先利用右手定則判斷通電導線各自產生的磁場強度,然后在利用矢量疊加的方式求解各個導體棒產生的磁場強度。
L1在ab兩點產生的磁場強度大小相等設為B1,方向都垂直于紙面向里,而L2在a點產生的磁場強度設為B2,方向向里,在b點產生的磁場強度也為B2,方向向外,規定向外為正,根據矢量疊加原理可知
B0−B1−B2=13B0B0−B1−B2=13B0
B2+B0−B1=12B0B2+B0−B1=12B0
可解得:B1=712B0B1=712B0 ;B2=112B0B2=112B0 故AC正確;故選AC
[點評]:【】:
磁場強度是矢量,對于此題來說ab兩點的磁場強度是由三個磁場的疊加形成,先根據右手定則判斷導線在ab兩點產生的磁場方向,在利用矢量疊加來求解即可。
【21題】
[答案]:B,D
[解析]: 利用電場力做功W=qUW=qU,可以找到兩點之間電勢差的關系,要知道中點電勢和兩端點電勢之間的關系。
A、選項根據題意無法判斷,故A項錯誤。
B、由于電場為勻強磁場,M為a、c連線的中點,N為b、d連線的中點,所以φM=φc−φc−φa2=φc+φa2φM=φc−φc−φa2=φc+φa2
φN=φd−φd−φb2=φd+φb2φN=φd−φd−φb2=φd+φb2
若該粒子從M點移動到N點,則電場力做功為
W=qUMN=q(φM−φN)=qφc+φa2−qφd+φb2=qUcd+qUab2=W1+W22W=qUMN=q(φM−φN)=qφc+φa2−qφd+φb2=qUcd+qUab2=W1+W22,故B正確;
C、因為不知道勻強電場方向,所以場強大小不是W2qLW2qL,故C錯誤;
D、若W1=W2,說明Ucd=UabUcd=Uab
UaM−UbN=(φa−φM)−(φb−φN)UaM−UbN=(φa−φM)−(φb−φN)
由因為φM=φc−φc−φa2=φc+φa2φM=φc−φc−φa2=φc+φa2;φN=φd−φd−φb2=φd+φb2φN=φd−φd−φb2=φd+φb2
解得:UaM−UbN=0UaM−UbN=0 ,故D正確;故選BD
[點評]:【】:
對勻強電場的電場特征要了解,利用電場力做功與電勢差之間的關系求解。
【22題】
[答案]: (1)如圖所示
(2)100;2910
[解析]: (1)R1的電阻比較小,所以R1與表頭并聯構成大量程的的電流表,R2的阻值比較大,與改裝后的電流表串聯可充當大量程的電壓表,設計電路圖如圖所示;

并聯后的總電阻為R′=90ΩR′=90Ω
要改裝3V電壓表需要串聯電阻,串聯電阻的阻值為[點評]:【】:
利用串并聯的關系求解改裝電表時需要串聯的電阻或者并聯的電阻大小。
【23題】
[答案]: (1)2.75
(2)如圖所示
(3)μ(M+m)g;μg
(4)0.40
[解析]: ①描點連線時要注意讓點均勻分布在線上或線的兩邊
②要結合圖像坐標整理出相應的數學函數,然后觀測斜率和截距分別代表什么。
(1)指針在2.7與2.8之間,估讀為2.75N2.75N
(2)描點畫線注意讓點均勻分布在線上或線的兩邊,作圖如下:

(3)木塊受到的是滑動摩擦力,根據滑動摩擦力的定義知f=μ(M+m)gf=μ(M+m)g
把公式化簡可得:f=μ(M+m)g=(μg)m+μMgf=μ(M+m)g=(μg)m+μMg
所以圖像的斜率k=μgk=μg
(4)取g=9.80 m/s2s2,取圖像上相距較遠的兩點求斜率k=2.94−2.160.25−0.05=3.9k=2.94−2.160.25−0.05=3.9
則μ=kg=3.99.8≈0.40μ=kg=3.99.8≈0.40
[點評]:【】:
在描點連線時要注意盡可能讓點在直線上,如果沒法在直線上也要均勻分布在直線的兩側,來減小誤差。
【24題】
[答案]: (1)vB′=3.0m/svB′=3.0m/s
(2)vA=4.3m/svA=4.3m/s
[解析]: 兩車碰撞過程動量守恒,碰后兩車在摩擦力的作用下做勻減速運動,利用運動學公式可以求得碰后的速度,然后在計算碰前A車的速度。
(1)設B車質量為mB,碰后加速度大小為aB,根據牛頓第二定律有
μmBg=mBaBμmBg=mBaB ①
式中μ是汽車與路面間的動摩擦因數。
設碰撞后瞬間B車速度的大小為vB′vB′,碰撞后滑行的距離為sBsB。由運動學公式有
vB′2=2aBsBvB′2=2aBsB ②
聯立①②式并利用題給數據得
vB′=3.0m/svB′=3.0m/s ③
(2)設A車的質量為mA,碰后加速度大小為aA。根據牛頓第二定律有
μmAg=mAaAμmAg=mAaA ④
設碰撞后瞬間A車速度的大小為vA′vA′,碰撞后滑行的距離為sAsA。由運動學公式有
vA′2=2aAsAvA′2=2aAsA ⑤
設碰撞后瞬間A車速度的大小為vAvA,兩車在碰撞過程中動量守恒,有
mAvA=mAvA′+mBvB′mAvA=mAvA′+mBvB′ ⑥
聯立③④⑤⑥式并利用題給數據得
vA=4.3m/svA=4.3m/s
[點評]:【】:靈活運用運動學公式及碰撞時動量守恒來解題。
【25題】
[答案]: (1)軌跡圖如圖所示:
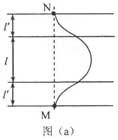
(2)v0=2El′Blv0=2El′Bl
(3)qm=43√El′B2l2qm=43El′B2l2;t′=BlE(1+3√πl18l′)t′=BlE(1+3πl18l′)
[解析]: (1)粒子在電場中做類平拋,然后進入磁場做圓周運動,再次進入電場做類平拋運動,結合相應的計算即可畫出軌跡圖
(2)在電場中要分兩個方向處理問題,一個方向做勻速運動,一個方向做勻加速運動。
(3)在磁場中的運動關鍵是找到圓心,求出半徑,結合向心力公式求解。
(1)粒子運動的軌跡如圖(a)所示。(粒子在電場中的軌跡為拋物線,在磁場中為圓弧,上下對稱)

(2)粒子從電場下邊界入射后在電場中做類平拋運動。設粒子從M點射入時速度的大小為v0,在下側電場中運動的時間為t,加速度的大小為a;粒子進入磁場的速度大小為v,方向與電場方向的夾角為θθ(見圖(b)),速度沿電場方向的分量為v1,根據牛頓第二定律有
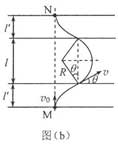
qE=ma ①
式中q和m分別為粒子的電荷量和質量,由運動學公式有
v1=at ②
l′=v0tl′=v0t ③
v1=vcosθv1=vcosθ ④
粒子在磁場中做勻速圓周運動,設其運動軌道半徑為R,由洛倫茲力公式和牛頓第二定律得
qvB=mv2RqvB=mv2R ⑤
由幾何關系得
l=2Rcosθl=2Rcosθ ⑥
聯立①②③④⑤⑥式得
v0=2El′Blv0=2El′Bl ⑦
(3)由運動學公式和題給數據得
v1=v0cotπ6v1=v0cotπ6 ⑧
聯立①②③⑦⑧式得
qm=43√El′B2l2qm=43El′B2l2 ⑨
設粒子由M點運動到N點所用的時間為t′t′,則
t′=2t+2(π2−π6)2πTt′=2t+2(π2−π6)2πT ⑩
式中T是粒子在磁場中做勻速圓周運動的周期,
T=2πmqBT=2πmqB ?
由③⑦⑨⑩?式得
t′=BlE(1+3√πl18l′)t′=BlE(1+3πl18l′) ?
[點評]:【】:
在復合場中的運動要分階段處理,每一個運動建立合理的公式即可求出待求的物理量。
【26題】
[答案]: (1)ZnS+3232O2(2)PbSO4
(3)調節溶液的pH
(4)無法除去雜質Fe2+
(5)Zn+Cd2+(7)溶浸
[解析]: (1)由于閃鋅礦的主要成分是ZnS,因此焙燒過程中主要反應的化學方程式為2ZnS+3O2(2)由于硫酸鉛不溶于水,因此濾渣1的主要成分除SiO2外還有PbSO4;要測定鐵離子,需要調節溶液的pH,又因為不能引入新雜質,所以需要利用氧化鋅調節pH,即氧化除雜工序中ZnO的作用是調節溶液的pH。根據表中數據可知沉淀亞鐵離子的pH較大,所以若不通入氧氣,其后果是無法除去雜質Fe2+。
(3)溶液中的Cd2+可用鋅粉除去,反應的離子方程式為Zn+Cd2+=Zn2++Cd。
(4)電解硫酸鋅溶液制備單質鋅時,陰極發生得到電子的還原反應,因此陰極是鋅離子放電,則陰極的電極反應式為Zn2++2e-=Zn;陽極是氫氧根放電,破壞水的電離平衡,產生氫離子,所以電解后還有硫酸產生,因此沉積鋅后的電解液可返回溶浸工序繼續使用。
[點評]:【分析】
焙燒時硫元素轉化為SO2,然后用稀硫酸溶浸,生成硫酸鋅、硫酸亞鐵和硫酸鎘,二氧化硅與稀硫酸不反應轉化為濾渣,由于硫酸鉛不溶于水,因此濾渣1中還含有硫酸鉛。由于沉淀亞鐵離子的pH較大,需要將其氧化為鐵離子,通過控制pH得到氫氧化鐵沉淀;濾液中加入鋅粉置換出Cd,較后將濾液電解得到金屬鋅,據此將解答。
【教育】
無機工業流程題能夠以真實的工業生產過程為背景,體現能力立意的命題為指導思想,能夠綜合考查學生各方面的基礎知識及將已有知識靈活應用在生產實際中解決問題的能力。解決本類題目的關鍵是分析流程中的每一步驟,可從以下幾個方面了解流程:①反應物是什么;②發生了什么反應;③該反應造成了什么后果,對制造產品有什么作用。即抓住一個關鍵點:一切反應或操作都是為獲得產品而服務的。另外本題中呈現的內容展示了中華科技成果對人類發展和社會進步的貢獻,可以引導學生自覺傳承我國科學文化,弘揚科學精神。
【27題】
[答案]: (1)247
(2)A
(3)1313
(4)劣于
(5)相對于催化劑X,催化劑Y積碳反應的活化能大,積碳反應的速率小;而消碳反應活化能相對小,消碳反應速率大
(6)AD
(7)pc(CO2)、pb(CO2)、pa(CO2)
[解析]: (1)已知:
①C(s)+2H2(g)=CH4(g) ΔH=-75 kJ•mol−1
②C(s)+O2(g)=CO2(g) ΔH=-394 kJ•mol−1
③C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ•mol−1
根據蓋斯定律可知③×2-②-①即得到該催化重整反應CH4(g)+CO2(g)=2CO(g)+2H2(g)的ΔH=+247 kJ•mol−1。正反應是體積增大的吸熱反應,所以有利于增強CH4平衡轉化率的條件是高溫低壓,答案選A;某溫度下,在體積為2 L的容器中加入2 mol CH4、1 mol CO2以及催化劑進行重整反應,達到平衡時CO2的轉化率是50%,根據方程式可知
CH4(g)+CO2(g)=2CO(g)+2H2(g)
起始濃度(mol/L) 1 0.5 0 0
轉化濃度(mol/L) 0.25 0.25 0.5 0.5
平衡濃度(mol/L) 0.75 0.25 0.5 0.5
所以其平衡常數為0.52×0.520.75×0.25=130.52×0.520.75×0.25=13mol2•L−2。
(2)①根據表中數據可知相對于催化劑X,催化劑Y積碳反應的活化能大,積碳反應的速率小;而消碳反應活化能相對小,消碳反應速率大,所以催化劑X劣于Y。A.正反應均是吸熱反應,升高溫度平衡向正反應方向進行,因此K積、K消均增加,A正確;B.升高溫度反應速率均增大,B錯誤;C.根據A中分析可知選項C錯誤;D.積碳量達到較大值以后再升高溫度積碳量降低,這說明v消增加的倍數比v積增加的倍數大,D正確。答案選AD。
②根據反應速率方程式可知在p(CH4)時,生成速率隨p(CO2)的升高而降低,所以根據圖像可知pa(CO2)、pb(CO2)、pc(CO2)從大到小的順序為pc(CO2)、pb(CO2)、pa(CO2)。
[點評]:【分析】
(1)根據蓋斯定律計算;根據反應特點結合溫度和壓強對平衡狀態的影響解答;根據轉化率利用三段式計算平衡常數;
(2)①根據活化能對反應的影響分析;根據反應熱結合溫度對平衡狀態的影響以及圖像曲線變化趨勢解答;
②根據反應速率方程式分析影響其因素結合圖像解答。
【教育】
本題主要是考查影響化學平衡的因素,化學圖像的分析與判斷,化學計算等知識。圖像分析是解答的易錯點和難點,注意化學平衡圖像分析的答題技巧,看圖像時:①一看面:縱坐標與橫坐標的意義;②二看線:線的走向和變化趨勢;③三看點:起點,拐點,終點,然后根據圖象中呈現的關系、題給信息和所學知識相結合,做出符合題目要求的解答。
【28題】
[答案]: (1)3FeC2O4+2K3[Fe(CN)6](2)隔絕空氣、使反應產生的氣體全部進入后續裝置
(3)CO2
(4)CO
(5)先熄滅裝置A、E的酒精燈,冷卻后停止通入氮氣
(6)取少許固體粉末于試管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液變紅色,證明含有Fe2O3
(7)粉紅色出現
(8)5cV×561000m×5cV×561000m×
[解析]: (1)光解反應的化學方程式為2K3[Fe(C2O4)3](2)①裝置中的空氣在高溫下能氧化金屬銅,能影響E中的反應,所以反應前通入氮氣的目的是隔絕空氣排盡裝置中的空氣;反應中有氣體生成,不會全部進入后續裝置。
②實驗中觀察到裝置B、F中澄清石灰水均變渾濁,說明反應中產生二氧化碳。裝置E中固體變為紅色,說明氧化銅被還原為銅,即有還原性氣體CO生成,由此判斷熱分解產物中含有CO2、CO;
③為防止倒吸,需要增加裝置中保持的壓力,所以停止實驗時應進行的操作是先熄滅裝置A、E的酒精燈,冷卻后停止通入氮氣即可。
④要檢驗Fe2O3存在首先要轉化為可溶性鐵鹽,因此方法是取少許固體粉末于試管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液變紅色,證明含有Fe2O3。
(3)①高錳酸鉀氧化草酸根離子,其溶液顯紅色,所以滴定終點的現象是粉紅色出現。
②鋅把鐵離子還原為亞鐵離子,酸性高錳酸鉀溶液又把亞鐵離子氧化為鐵離子。反應中消耗高錳酸鉀是0.001cVmol,Mn元素化合價從+7價降低到+2價,所以根據電子得失守恒可知鐵離子的物質的量是0.005cVmol,則該晶體中鐵的質量分數的表達式為0.005cV×56m×=5cV×561000m×0.005cV×56m×=5cV×561000m×。
[點評]:【分析】
(1)根據亞鐵離子能與K3[Fe(CN)6]發生顯色反應解答;
(2)①根據氮氣能隔絕空氣和排盡氣體分析;
②根據CO2、CO的性質分析;
③要防止倒吸可以根據外界條件對壓強的影響分析;
③根據鐵離子的檢驗方法解答;
(3)①根據酸性高錳酸鉀溶液顯紅色 ;
②根據電子得失守恒計算。
【教育】
本題主要是考查物質分解產物檢驗、元素含量測定等實驗方案設計與評價,題目難度中等,明確實驗原理和相關物質的性質是解答的關鍵。關于化學實驗從安全角度常考慮的主要因素如下:凈化、吸收氣體及熄滅酒精燈時要防止液體倒吸;進行某些易燃易爆實驗時要防爆炸(如H2還原CuO應先通H2,氣體點燃前先驗純等);防氧化(如H2還原CuO后要“先滅燈再停氫”,白磷切割宜在水中進行等);污染性的氣體要進行尾氣處理;有粉末狀物質參加的反應,要注意防止導氣管堵塞;防吸水(如實驗取用、制取易吸水、潮解、水解的物質時宜采取需要措施,以增加達到實驗目的)。
【29題】
[答案]: (1). ①手術但不切除垂體;切除垂體;③每隔時間,測定并記錄兩組大鼠的體重
(2). 生長;促甲狀腺
[解析]: 本題采用切除法,以“研究垂體對機體生長發育的作用”為情境,考查考生的實驗與探究能力。解題的關鍵是由題意準確把握實驗目的(研究垂體對機體生長發育的作用),進而明辨實驗變量(自變量、因變量、無關變量)。在此基礎上,依據實驗設計應遵循的原則,圍繞給出的不完善的實驗步驟,以及垂體分泌的與生長發育有關的激素等知識,對各問題情境進行解答。
【詳解】
(1)依題意可知:本實驗的自變量是垂體的有無,因變量是通過檢測幼齡大鼠的體重變化來反映其生長發育的狀況,其他對實驗結果有影響的因變量應控制相同且適宜。據此結合題意所示的實驗方法(切除法)、不完善的實驗步驟和實驗設計應遵循的原則可知,①A組(對照組) 手術但不切除垂體,B組(實驗組)要切除垂體;③的內容為“每隔時間,測定并記錄兩組大鼠的體重”。
(2)垂體分泌的促甲狀腺激素可促進甲狀腺的正常生長發育,調節甲狀腺激素的合成和分泌。垂體分泌的生長激素和甲狀腺分泌的甲狀腺激素都有促進生長發育的作用,但前者主要促進生長,后者主要促進發育,二者共同協調,機體才能正常的生長發育。可見,若B組大鼠生長發育的狀況不如A組,則是由于B組的處理使大鼠缺失了來源于垂體的生長激素和促甲狀腺激素。
[點評]:【】
解答實驗題的切入點為找準實驗目的,由此分析出實驗的自變量和因變量,從而做到在實驗設計或完善實驗步驟中有的放矢。實驗處理要遵循“單一變量和對照原則”,設立實驗組和對照組時,注意控制無關變量,在措辭中往往有“相同”、“一致”等字眼;在培養(或飼養)、觀察記錄實驗現象或記錄測定的實驗數據時,依然在措辭中體現對無關變量的控制,經常有“相同條件下”、“每隔時間”等字眼。把握上述要點,本題便可形成如下清晰的實驗思路:
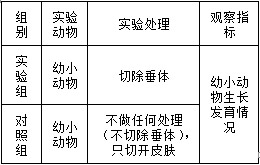
實驗動物選取分組時,要選取生長發育狀況相同的,且飼養時其他條件要一致。
【30題】
[答案]: (1). 下層;A葉片的凈光合速率達到較大時所需光照強度低于B葉片
(2). 暗
(3). 無水乙醇
[解析]: 本題以反映實驗結果的曲線圖為情境,綜合考查考生對綠葉中色素的提取、光合作用過程及其影響因素等相關知識的識記和理解能力。解題的關鍵是理解橫縱坐標的含義,把握曲線走勢。在此基礎上結合題意并從圖示中提取信息,圍繞光合作用的過程及其影響的環境因素等相關知識,對各問題情境進行分析解答。
【詳解】
(1)由于上層葉片對陽光的遮擋,導致下層葉片接受的光照強度較弱,因此下層葉片凈光合速率達到較大值時所需要的光照強度較上層葉片低,據此分析圖示可推知:A葉片是樹冠下層的葉片。
(2)光合作用包括光反應和暗反應兩個階段,氧氣產生于光反應階段。光照強度達到數值時,A葉片的凈光合速率開始下降,但測得放氧速率不變,說明光反應速率不變,則凈光合速率降低的主要原因是光合作用的暗反應受到抑制。
(3)綠葉中的葉綠素等光合色素能夠溶解在有機溶劑無水乙醇中,可以用無水乙醇提取葉綠素。
[點評]:【】
坐標曲線題的解題關鍵是:①要理解橫、縱坐標的含義及曲線代表的含義,這是解題的重心所在。②關注坐標上的“四點、二量、一趨勢”。“四點”指的是起點、交點、折點和終點;“二量”指的是分清自變量與因變量,不能顛倒;“一趨勢”,指的是曲線的走勢,特別要注意的是分析問題時要結合橫軸的點、區段來進行。③分析曲線變化有關的知識點時,還要挖掘或捕捉題目所給予的有效信息。
【31題】
[答案]: (1). 生產者固定的能量在沿食物鏈流動過程中大部分都損失了,傳遞到下一營養級的能量較少
(2). 甲對肉食性動物的恐懼程度比乙高,肉食性動物引入后甲逃離該生態系統的數量比乙多
(3). 大型肉食性動物捕食野豬;野豬因恐懼減少了采食。
[解析]: 大型肉食性動物對低營養級肉食性動物與植食性動物的捕食和驅趕,會對群落或生態系統產生影響,據此,以這一建立在“威懾”與“恐懼”基礎上的種間關系(捕食和驅趕)為切入點并與生態系統的能量流動建立聯系,結合題意,對相應問題進行解答。
【詳解】
(1)生產者固定的太陽能總量是流入一個生態系統的總能量?能量在沿著食物鏈和食物網流動的過程中,各個營養級的生物都會通過自身的呼吸作用而消耗一部分能量(以熱能的形式散失),余下的用于生長發育和繁殖等生命活動的能量中,也有一部分隨著殘枝敗葉或遺體殘骸等被分解者分解釋放出來而不能輸入到下一營養級,即生產者固定的能量在沿食物鏈流動的過程中大部分損失了,傳遞到下一營養級的能量較少,因此食物鏈中的營養級數量一般不會太多。
(2)依題意可知:肉食性動物的引入,使得甲、乙兩種植食性動物間的競爭結果發生了反轉(甲的數量優勢地位喪失),而該反轉不是由于肉食性動物的直接捕食造成的,進而推知,甲的數量優勢地位喪失的可能原因是:肉食性動物對甲、乙的驅趕作用而引起的甲、乙的“恐懼”程度不同,甲對肉食性動物的“恐懼”程度比乙高,肉食性動物引入后甲逃離該生態系統的數量比乙多。
(3)某種大型肉食性動物在某地區的森林中重新出現,會減輕該地區野豬對農作物的破壞程度,由題意中“恐懼生態學”的知識可推知,其可能的原因有:一是該種大型肉食性動物對野豬的直接捕食而導致野豬的個體數減少,二是野豬因“恐懼”減少了采食。
[點評]:【】
本題的難點在于對(2)(3)的解答。解題的關鍵是準確把握題意中“恐懼生態學”知識的內涵,抓住“捕食和驅趕”這一關鍵信息,并結合題意分析大型肉食性動物對相應的低營養級動物種群數量的影響。
【32題】
[答案]: (1). ZAZA,ZaW;ZAW、ZAZa,雌雄均為正常眼;1/2
(2). 雜交組合:豁眼雄禽(ZaZa)×正常眼雌禽(ZAW)
預期結果:子代雌禽為豁眼(ZaW),雄禽為正常眼(ZAZa)
(3). ZaWmm;ZaZaMm,ZaZamm
[解析]: 理清“基因的分離定律、伴性遺傳、基因的自由組合定律”等相關知識,形成清晰的知識網絡。在此基礎上,依據上述相關知識并圍繞題意,準確定位親本的基因型,推知子代(F1或F2)的基因型、表現型及其相應的性狀分離比,進而對相關問題進行解答。
【詳解】
(1)依題意可知,在家禽中,雄性的性染色體組成為ZZ,雌性的性染色體組成為ZW,豁眼性狀由Z染色體上的隱性基因a控制,且在W染色體上沒有其等位基因。由此推知,親本純合體正常眼雄禽的基因型為ZAZA,親本豁眼雌禽的基因型為ZaW,二者雜交所得F1的基因型為ZAZa、ZAW,F1的雌雄個體均為正常眼。F1的雌雄個體交配,所得F2的基因型及其比例為ZAZA∶ZAZa∶ZAW∶ZaW=1∶1∶1∶1,可見,F2雌禽中豁眼禽(ZaW)所占的比例為1/2。
(2)雌性親本將Z染色體遺傳給子代的雄性,將W染色體遺傳給子代的雌性,而子代的雌性的Z染色體則來自雄性親本。可見,若使子代中的雌禽均為豁眼(ZaW)、雄禽均為正常眼(ZAZ-),則親本的雜交組合為:豁眼雄禽(ZaZa)×正常眼雌禽(ZAW);該雜交組合產生的子代的基因型為ZAZa、ZaW,表現型為:子代雌禽均為豁眼(ZaW),雄禽均為正常眼(ZAZa)。
(3)依題意可知:m基因純合時可使部分應表現為豁眼的個體表現為正常眼,而MM和Mm對個體眼的表現型無影響。兩只表現型均為正常眼的親本交配,其子代中出現豁眼雄禽,這說明子代中還存在正常眼雄禽(ZAZ-);因子代出現的豁眼雄禽的基因型為ZaZa,所以親本雌禽必然含有Za,進而推知該親本雌禽的基因型為ZaWmm,親本雄禽的基因型為ZAZaMM或ZAZaMm或ZAZamm,子代中豁眼雄禽可能的基因型包括ZaZaMm、ZaZamm。
[點評]:【】
雞的性別決定方式為ZW型,公雞的性染色體組成為ZZ,母雞的性染色體組成為ZW;基因的分離定律研究的是一對等位基因在傳宗接代中的傳遞規律,若該對等位基因位于性染色體上,則同時還表現為伴性遺傳;基因的自由組合定律研究的是位于非同源染色體上的非等位基因在傳宗接代中的傳遞規律。據此以題意“Z染色體上的隱性基因a”和“M/m基因位于常染色體上”等信息為切入點,明辨相應基因在遺傳時所遵循的遺傳規律,有針對性地進行分析解答。
【33題】
[答案]:B,D,E
[解析]: ABCE:氣體的內能等于分子熱運動動能和分子之間勢能的總和,故AC錯,BE對;
D:根據熱力學第律ΔU=W+QΔU=W+Q知道,改變內能的方式有做功和熱傳遞,所以體積發生變化時,內能可能不變,故D正確;故選BDE
[點評]:【】:
不僅要知道內能是什么,還要知道改變內能的方式是什么。
【34題】
[答案]: W=(p0S+mg)hW=(p0S+mg)h
[解析]: 由于活塞處于平衡狀態所以可以利用活塞處于平衡狀態,求封閉氣體的壓強,然后找到不同狀態下氣體參量,計算溫度或者體積。
開始時活塞位于a處,加熱后,汽缸中的氣體先經歷等容過程,直至活塞開始運動。設此時汽缸中氣體的溫度為T1,壓強為p1,根據查理定律有
p0T0=p1T1p0T0=p1T1①
根據力的平衡條件有
p1S=p0S+mgp1S=p0S+mg②
聯立①②式可得
T1=(1+mgp0S)T0T1=(1+mgp0S)T0③
此后,汽缸中的氣體經歷等壓過程,直至活塞剛好到達b處,設此時汽缸中氣體的溫度為T2;活塞位于a處和b處時氣體的體積分別為V1和V2。根據蓋—呂薩克定律有
V1T1=V2T2V1T1=V2T2④
式中
V1=SH⑤
V2=S(H+h)⑥
聯立③④⑤⑥式解得
T2=(1+hH)(1+mgp0S)T0T2=(1+hH)(1+mgp0S)T0⑦
從開始加熱到活塞到達b處的過程中,汽缸中的氣體對外做的功為
W=(p0S+mg)hW=(p0S+mg)h⑧
[點評]:【】:
本題的關鍵是找到不同狀態下的氣體參量,再利用氣態方程求解即可。
【35題】
[答案]: 365;2451724517
[解析]: 可以假設橋的長度,分別算出運動時間,結合題中的1s求橋長,在不同介質中傳播時波的頻率不會變化。
(1)設橋的長度為s
則聲音在鋼鐵中傳播的時間t=sv=s4900t=sv=s4900
聲音在空氣中的傳播時間為t′=sv′=s340t′=sv′=s340
根據題意Δt=t′−t=s340−s4900=1Δt=t′−t=s340−s4900=1
解得:s=365ms=365m
(2)聲音在不同介質中的頻率是不會改變的,由公式可知λ=vfλ=vf ,[點評]:【】:
本題考查了波的傳播的問題,知道不同介質中波的傳播速度不同,當傳播是的頻率不會發生變化。
【36題】
[答案]: (1)δ=60°
(2)23√3≤n≤2233≤n≤2
[解析]: (1)根據題意畫出光路圖,根據幾何關系找到出射光線與入射光線之間的夾角;
(2)要增加在E點發生全反射,則在E點的入射角要大于等于臨界角C
(ⅰ)光線在BC面上折射,由折射定律有
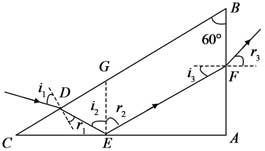
sini1=nsinr1sini1=nsinr1①
式中,n為棱鏡的折射率,i1和r1分別是該光線在BC面上的入射角和折射角。光線在AC面上發生全反射,由反射定律有
i2=r2②
式中i2和r2分別是該光線在AC面上的入射角和反射角。光線在AB面上發生折射,由折射定律有
nsini3=sinr3nsini3=sinr3③
式中i3和r3分別是該光線在AB面上的入射角和折射角。由幾何關系得
i2=r2=60°,r1=i3=30°④
F點的出射光相對于D點的入射光的偏角為
δ=(r1–i1)+(180°–i2–r2)+(r3–i3)⑤
由①②③④⑤式得
δ=60°⑥
(ⅱ)光線在AC面上發生全反射,光線在AB面上不發生全反射,有
nsini2≥nsinC>nsini3nsini2≥nsinC>nsini3⑦
式中C是全反射臨界角,滿足
nsinC=1nsinC=1⑧
由④⑦⑧式知,棱鏡的折射率n的取值范圍應為
23√3≤n≤2233≤n≤2⑨
[點評]:【】:
本題考查了幾何光學,處理此類題的方法一般是正確畫光路圖利用幾何關系求偏角,還要知道全發射的條件是什么。
【37題】
[答案]: (1)(2)啞鈴(紡錘)
(3)H2S
(4)S8相對分子質量大,分子間范德華力強
(5)平面三角
(6)2
(7)sp3
(8)4MNAa3×10214MNAa3×1021
(9)2√2a22a
[解析]: (1)基態Fe原子的核外電子排布式為1s22s22p63s23p63d64s2,則其價層電子的電子排布圖(軌道表達式)為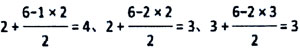
(3)S8、二氧化硫形成的晶體均是分子晶體,由于S8相對分子質量大,分子間范德華力強,所以其熔點和沸點要比二氧化硫的熔點和沸點高很多;
(4)氣態三氧化硫以單分子形式存在,根據(2)中分析可知中心原子含有的價層電子對數是3,且不存在孤對電子,所以其分子的立體構型為平面三角形。分子中存在氧硫雙鍵,因此其中共價鍵的類型有2種,即σ鍵、π鍵;固體三氧化硫中存在如圖(b)所示的三聚分子,該分子中S原子形成4個共價鍵,因此其雜化軌道類型為sp3。
(5)根據晶胞結構可知含有鐵原子的個數是12×1/4+1=4,硫原子個數是8×1/8+6×1/2=4,晶胞邊長為a nm、FeS2相對式量為M,阿伏加德羅常數的值為NA,則其晶體密度的計算表達式為ρ=mV=4MNA(a×10−7)3g/cm3=4MNAa3×1021g/cm3ρ=mV=4MNA(a×10−7)3g/cm3=4MNAa3×1021g/cm3;晶胞中Fe2+位于S2−2S22−所形成的正八面體的體心,該正八面體的邊長是面對角線的一半,則為2√2a22anm。
[點評]:【分析】
(1)根據鐵、硫的核外電子排布式解答;
(2)根據價層電子對互斥理論分析;
(3)根據影響分子晶體熔沸點高低的是分子間范德華力判斷;
(4)根據價層電子對互斥理論分析;
(5)根據晶胞結構、結合密度表達式計算。
【教育】
本題主要是考查核外電子排布、雜化軌道、空間構型、晶體熔沸點比較以及晶胞結構判斷與計算等,難度中等。其中雜化形式的判斷是難點,由價層電子特征判斷分子立體構型時需注意:價層電子對互斥模型說明的是價層電子對的立體構型,而分子的立體構型指的是成鍵電子對的立體構型,不包括孤電子對。①當中心原子無孤電子對時,兩者的構型一致;②當中心原子有孤電子對時,兩者的構型不一致;價層電子對互斥模型能推測分子的幾何構型,但不能解釋分子的成鍵情況,雜化軌道理論能解釋分子的成鍵情況,但不能推測分子的幾何構型。兩者相結合,具有的互補性,可達到處理問題簡便、迅速、的效果。
【38題】
[答案]: (1)C6H12O6
(2)羥基
(3)取代反應
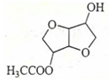
(4)
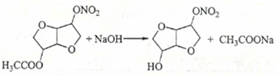
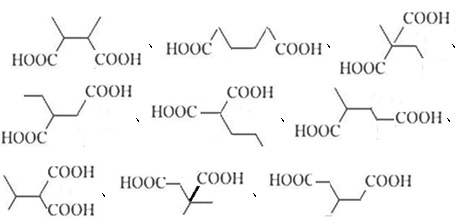
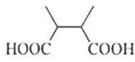
(6)9
(7)[解析]: (1)葡萄糖的分子式為C6H12O6。
(2)葡萄糖在催化劑作用下與氫氣發生醛基的加成反應生成A,因此A中含有的官能團的名稱為羥基。
(3)由B到C發生酯化反應,反應類型為取代反應。
(4)根據B的結構簡式可知C的結構簡式為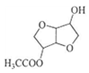
[點評]:【分析】
葡萄糖在催化劑作用下與氫氣發生醛基的加成反應生成A,A在濃硫酸的作用下發生分子內脫水反應生成B,B與乙酸發生酯化反應生成C,根據C與D的分子式可知C生成D是C分子中另一個羥基與硝酸發生酯化反應,D在氫氧化鈉溶液中水解生成E,據此解答。
【教育】
高考化學試題中對有機化學基礎的考查題型比較固定,通常是以生產、生活的陌生有機物的合成工藝流程為載體考查有機化學的知識,涉及常見有機物官能團的結構、性質及相互轉化關系,涉及有機物結構簡式的確定、反應類型的判斷、化學方程式的書寫、同分異構體的識別和書寫等知識的考查。它要求學生能夠通過題給情境中適當遷移,運用所學知識分析、解決實際問題,這高考有機化學復習備考的方向。本題的難點是同分異構體數目判斷,同分異構體類型通常有:碳鏈異構、官能團異構、位置異構等,有時還存在空間異構,要充分利用題目提供的信息來書寫符合題意的同分異構體。對于二元取代物同分異構體的數目判斷,可固定一個取代基的位置,再移動另一取代基的位置以確定同分異構體的數目,本題就是采用這種方法。
【39題】
[答案]: (1). 可以
(2). 在達到消毒目的的同時,營養物質損失較少
(3). 破壞DNA結構;消毒液
(4). 氯氣
(5). 未將鍋內冷空氣排盡
[解析]: 由題意“通過消毒和滅菌來避免雜菌的污染”可知,本題考查的是“無菌技術”。理清實驗室和日常生產、生活中常用的消毒和滅菌方法是解答此題的關鍵。
【詳解】
(1)能耐高溫的、需要保持干燥的物品,如玻璃器皿(吸管、培養皿)和金屬用具等可以放入干熱滅菌箱中進行干熱滅菌。
(2)煮沸消毒法即在100℃煮沸5~6 min可以殺死微生物細胞和一部分芽孢;巴氏消毒法即在70~75℃煮30 min或在80℃煮15min,可以殺死微生物,并且增加營養物質不被破壞。因此,與煮沸消毒法相比,牛奶消毒常采用的巴氏消毒法或高溫瞬時消毒法的優點是在達到消毒目的的同時,營養物質損失較少。
(3)因紫外線能破壞DNA結構,所以密閉空間內的空氣可采用紫外線照射消毒。在照射前,適量噴灑消毒液,可強化消毒效果。
(4)通常乙醇消毒是75%的酒精,有氣味,影響水質,不適宜消毒自來水;高錳酸鉀本身有顏色,消毒后溶液呈紫紅色,無法使用;因此水廠供應的自來水通常是經過氯氣消毒的。
(5)采用高壓蒸汽滅菌時,鍋內的水加熱煮沸,將其中原有的冷空氣徹底排除后才能將鍋密閉。如果未將鍋內冷空氣排盡,則會出現壓力達到設定要求,而鍋內并沒有達到相應溫度的現象。
[點評]:【】
(1)消毒與滅菌的區別:
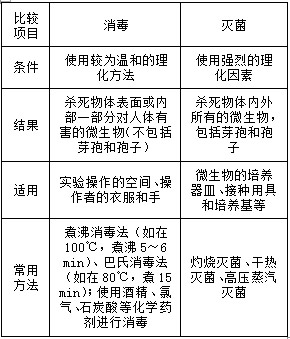
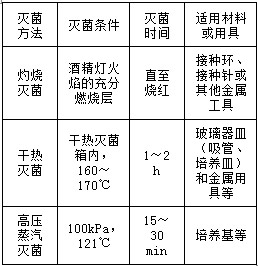
(2)三種常用滅菌方法的比較:
【40題】
[答案]: (1). E1和E4;甲的完整;甲與載體正確連接
(2). 轉錄;翻譯
(3). 細胞核;去核卵母細胞
(4). 核DNA
[解析]: 本題以圖文結合的形式綜合考查學生對基因工程、核移植等相關知識的識記和理解能力。解答本題需熟記并理解核移植技術的過程、基因工程的基本操作程序,特別是明確PCR技術的原理和過程、基因表達載體的組成及其作用、限制酶的作用等相關知識并形成清晰的知識網絡。在此基礎上,結合問題情境,從題圖中提取有效信息進行相關問題的解答。
【詳解】
(1)要增加目的基因在受體細胞中能夠正確表達,目的基因的首端應有啟動子,尾端應有終止子。甲是將某種病毒的外殼蛋白(L1)基因連接在GFP基因的5ˊ末端而獲得的L1-GFP融合基因,據此結合題意并分析圖示可知:該團隊在將甲插入質粒P0時,如果用E2或E3,則目的基因不完整,而使用E1和E4這兩種限制酶進行酶切增加了甲的完整,而且也增加了甲與載體正確連接,因此,使用的兩種限制酶,是E1和E4。
(2)構建的真核表達載體P1中含有GFP基因,而GFP基因的表達產物“某種熒光蛋白(GFP)”在紫外光或藍光激發下會發出綠色熒光。若在導入P1的牛皮膚細胞中觀察到了綠色熒光,則說明L1基因在牛的皮膚細胞中完成了表達。基因的表達過程包括轉錄和翻譯。
(3)若要獲得含有甲的牛,可采用核移植技術,即將能夠產生綠色熒光細胞的細胞核移入牛的去核卵母細胞中獲得重組細胞,并將該重組細胞在體外培養成重組胚胎,再經過胚胎移植等獲得含有甲的牛。
(4)PCR是多聚酶鏈式反應的縮寫,是一種在生物體外復制特定DNA片斷的核酸合成技術。若利用PCR方法檢測甲是否存在于克隆牛的不同組織細胞中,則應分別以該牛不同組織細胞中的核DNA作為PCR模板。
[點評]:【】
本題的難點在于對(1)的解答。解題的關鍵是:以題意“獲得L1-GFP融合基因(簡稱為甲)”的過程為切入點,圍繞“基因表達載體的組成及其作用”和圖示呈現的“酶切位點的”信息進行綜合分析。
以上就是伊頓教育網小編為大家整理的2018年卷2的理科綜合試題,2019年的理科考生作為參考,希望大家在考場上考出好成績!加油吧!
- 熱門課程
- 熱門資訊
- 熱門資料
- 熱門福利
-
 渭南宏帆廣場附近有秦學伊頓校區嗎?一對一怎么收費?【摘要】渭南屬于二線城市,教育資源相對來說也是很豐富的,渭南有很多補習機構,不管是口碑還是教學質量還是升學率都做的非常好。很多家長了解補習機構的目的就是希望能夠找一個性價比不錯而且學生能提分的,那么本期咱們就推薦秦學伊頓的一對一,給各位家長開開眼啦!
渭南宏帆廣場附近有秦學伊頓校區嗎?一對一怎么收費?【摘要】渭南屬于二線城市,教育資源相對來說也是很豐富的,渭南有很多補習機構,不管是口碑還是教學質量還是升學率都做的非常好。很多家長了解補習機構的目的就是希望能夠找一個性價比不錯而且學生能提分的,那么本期咱們就推薦秦學伊頓的一對一,給各位家長開開眼啦! -
 咸陽伊頓教育升學率咋樣?適合初三沖刺嗎?【摘要】咸陽伊頓教育的升學率情況以及班型還有口碑,一直都是咸陽的家長非常關心的問題,許多家長到了即將中高考的時候,總會不厭其煩的想花幾萬塊錢給孩子報名沖刺班,只要孩子的分數能有所長進,本期,咱們就針對最近咸陽家長都非常關心的咸陽伊頓教育展開聊聊那!
咸陽伊頓教育升學率咋樣?適合初三沖刺嗎?【摘要】咸陽伊頓教育的升學率情況以及班型還有口碑,一直都是咸陽的家長非常關心的問題,許多家長到了即將中高考的時候,總會不厭其煩的想花幾萬塊錢給孩子報名沖刺班,只要孩子的分數能有所長進,本期,咱們就針對最近咸陽家長都非常關心的咸陽伊頓教育展開聊聊那! -
 高三一對一輔導推薦哪家?西安大唐學校口碑咋樣?【摘要】高三階段即將面臨高考,許多準高三生的家長也已經慢慢把目光轉移到了課外補習機構上,他們想提前讓孩子步入復習的進程中,所以往往會選擇一對一或者沖刺班的形式給孩子補課。本期,我們就來分析最近很受歡迎的西安大唐學校吧!
高三一對一輔導推薦哪家?西安大唐學校口碑咋樣?【摘要】高三階段即將面臨高考,許多準高三生的家長也已經慢慢把目光轉移到了課外補習機構上,他們想提前讓孩子步入復習的進程中,所以往往會選擇一對一或者沖刺班的形式給孩子補課。本期,我們就來分析最近很受歡迎的西安大唐學校吧! -
 丁準全日制學校咨詢電話多少?西安碑林區有校區嗎?【摘要】全日制補習學習學校的好處就是管理嚴格,讓學生在吃住學一體化的環境里專注起來,然后提高成績,丁準全日制學校的口碑這些年一直都是西安同類型補習機構里不錯的,那么它的咨詢電話多少?有沒有其他校區呢?今天咱們就來做個簡單介紹!
丁準全日制學校咨詢電話多少?西安碑林區有校區嗎?【摘要】全日制補習學習學校的好處就是管理嚴格,讓學生在吃住學一體化的環境里專注起來,然后提高成績,丁準全日制學校的口碑這些年一直都是西安同類型補習機構里不錯的,那么它的咨詢電話多少?有沒有其他校區呢?今天咱們就來做個簡單介紹!
-
 高考作文素材積累:流浪詩人——我的人生之路各位學生注意了,現在就要進入到2023年陰歷新年,各位學生過完年距離中高考又進了一步,為方便大家能夠積累更多的作文素材,小編老師為定期為大家更新優秀范文,下面大家一起來賞析“流浪詩人——我的人生之路”。 作文題 閱讀下面的材料,根據要求寫一篇不少于800字的文章。(60分) 黃大發,一位普
高考作文素材積累:流浪詩人——我的人生之路各位學生注意了,現在就要進入到2023年陰歷新年,各位學生過完年距離中高考又進了一步,為方便大家能夠積累更多的作文素材,小編老師為定期為大家更新優秀范文,下面大家一起來賞析“流浪詩人——我的人生之路”。 作文題 閱讀下面的材料,根據要求寫一篇不少于800字的文章。(60分) 黃大發,一位普 -
 2023年高考作文素材積累:“絕品即常品”各位學生大家覺得高考作文多少分才過關呢?小編老師覺得作文滿分60分大家作文在56分以上才算是過關,大家都知道高考一分之差差之千里,大家不要放過任何一個可以提分的可能!為幫助大家積累素材,小編老師為大家整理了比較好的作文題目和作文范文,供大家參考! 作文題 閱讀下面的材料,根據要求寫一篇不
2023年高考作文素材積累:“絕品即常品”各位學生大家覺得高考作文多少分才過關呢?小編老師覺得作文滿分60分大家作文在56分以上才算是過關,大家都知道高考一分之差差之千里,大家不要放過任何一個可以提分的可能!為幫助大家積累素材,小編老師為大家整理了比較好的作文題目和作文范文,供大家參考! 作文題 閱讀下面的材料,根據要求寫一篇不 -
 高考英語素材,高考英語作文開頭常用句子高考英語素材,高考英語作文開頭常用句子!一提到英文寫作,很多同學就頭疼,如何組織語言、如何下筆呢?但自從知道了一些萬能的“套話”你就會發現自己的寫作水平會更上一層樓!下面小編老師為大家整理了高考英語作文開頭常用句子,想要了解的學生收藏起來! 開頭常用句子 1.Depending on per
高考英語素材,高考英語作文開頭常用句子高考英語素材,高考英語作文開頭常用句子!一提到英文寫作,很多同學就頭疼,如何組織語言、如何下筆呢?但自從知道了一些萬能的“套話”你就會發現自己的寫作水平會更上一層樓!下面小編老師為大家整理了高考英語作文開頭常用句子,想要了解的學生收藏起來! 開頭常用句子 1.Depending on per -
 西安高三化學輔導班哪家好?化學現在在新高考的分量也比較重,很多專業都要求選擇化學這門課。與物理相比化學不算難。最近有學生問老師西安高三化學輔導班哪家好?下面,小編老師為大家推薦西安一家比較好的高中補習機構,大家了解一下: 伊頓教育高三·化學輔導 基礎 1.激發學習動機2.培養學習興趣3.化學方程式總結歸納
西安高三化學輔導班哪家好?化學現在在新高考的分量也比較重,很多專業都要求選擇化學這門課。與物理相比化學不算難。最近有學生問老師西安高三化學輔導班哪家好?下面,小編老師為大家推薦西安一家比較好的高中補習機構,大家了解一下: 伊頓教育高三·化學輔導 基礎 1.激發學習動機2.培養學習興趣3.化學方程式總結歸納


















 All right reserved
All right reserved
